Přestože se ke konzumaci dusičnanů vážou jistá rizika, v přiměřeném množství má jejich příjem prokazatelně pozitivní vliv na zdraví. Jídelníček bohatý na zdroje NO (především v podobě zeleniny) je prospěšný pro zdraví kardiovaskulárního systému a působí jako prevence kardiovaskulárních potíží (Bailey et. al, 2010a). U jedinců se sníženou výchozí zdatností pro zvládnutí efektivní cvičební jednotky by mohla suplementace (doplňování stravy) nitráty ulehčit počáteční snažení o zlepšení zdatnosti do té doby, než dojde k potřebné adaptaci mechanismů způsobujících vazodilataci. Cvičení by tak mohlo být zvladatelnější i pro pacienty, kteří nejsou pravidelně trénovaní a z důvodu choroby fyzickou aktivitu špatně snášejí (Asano, 2012, p. 80).
Suplementace nitráty prokazatelně zesiluje některé funkce oxidu dusnatého, dokonce i u zdravých lidí. Na příklad lze dosáhnout snížení krevního tlaku i u jedinců s normálními hodnotami krevního tlaku (AIS, 2011, p. 2).
Zajímavá je na využití nitrátu z potravin jako doplňku stravy jeho jednoduchost. Není třeba užívat farmaceutické produkty obsahující potenciálně nebezpečné dusitany. K dosažení pozitivních účinků nitrátu stačí vytvořit koncentrovaný džus ze zeleniny s vysokým obsahem dusičnanů. Za předpokladu, že by se prokázaly pozitivní účinky nitrátu ze zeleniny, by tento nápoj mohl být konzumován pro podporu kardiovaskulárního zdraví v rámci obvyklého jídelníčku. Vědecká pracoviště po celém světě se zajímají o účinky dietních nitrátů a zkoumají jejich využití pro usnadnění fyzické aktivity. K výzkumu jsou používány jak nápoje obsahující nitrát (NO3-), tak L-arginin. Dosud bylo dosaženo velice zajímavých výsledků (viz dále). Pro efektivitu suplementace je nutné se vyznat v dávkování nitrátu.
Dávkování
V aktuálních studiích se používané množství nitrátu na jednu dávku pohybuje od 300 mg NO3- až po cca 700 mg NO3 - (5–11 mmol/L). Pro nitrát platí: 1 mmol = 62 mg NO3- (AIS, 2011, p. 2). Evropský úřad pro bezpečnost potravin stanovuje akceptovatelný denní příjem na 3,7 mg NO/kg tělesné váhy (EFSA, 2008). Používají se dva způsoby dávkování. Tím prvním je konzumace 500 ml řepného džusu nebo jiného adekvátního zdroje nitrátu 2–2,5 hodiny před cvičením v případě 1 denní intervence (AIS, 2011). Druhým způsobem je podávání stejné účinné dávky 6 po sobě následujících dnů, s možností pití v průběhu dne (Bailey et al, 2009).
Červená řepa
Jako zdroj dietního nitrátu je často používána červená řepa. Řepný džus, především v koncentrované formě a ve větších dávkách někdy způsobuje mírný gastrointestinální diskomfort a jeho konzumace se často projevuje dočasným růžovým zabarvením moči a stolice. Tento vedlejší efekt je neškodný. Výhodou využití červené řepy je fakt, že je již odzkoušena na mnoha studiích a zatím se výborně osvědčila bez negativních vedlejších účinků (AIS, 2011, p. 3).
Jak oblíbenost džusu z červené řepy začala stoupat, postupně se na světovém trhu objevovaly sériově vyráběné džusy z červené řepy. Tento rozmach usnadnil další zkoumání účinků nitrátu, protože již nebylo třeba vyrábět si vlastní zdroj dusičnanů a testovat ho na obsahové látky. Přípravou domácího zeleninového přípravku ze zeleniny bohaté na dusičnany nemusí být nutně dosaženo potřebné dávky nitrátu, pro účely výzkumu je tak jistější a jednodušší pořídit si některý z prodávaných produktů. Pro provedení dvojitě zaslepených studií je nutné mít kromě suplementačního přípravku také kvalitní placebo. Patentovaná příprava nitrátů zbaveného řepného džusu umožňuje, použití efektivní kontroly placebem, pro studie zkoumající účinek zeleninových zdrojů dusičnanu (AIS, 2011).
AIS jako možný zdroj nitrátu uvádí i dusičnan sodný. V případě jeho použití je nutné dávat pozor na nepřiměřené dávky. V případě neúmyslné záměny za dusitan sodný se člověk vystavuje značnému zdravotnímu riziku (AIS, 2011, p. 2).
Další potravinové zdroje
Dusičnany se na Zemi vyskytují zcela přirozeně. Na naší planetě jsou od nepaměti, jak ve vodě, tak v půdě a dnes tomu není jinak. V posledních desetiletích se však jejich výskyt v přírodě uměle zvýšil přímými zásahy člověka. Přirozený obsah dusičnanů v půdě a ve vodě je dán koloběhem dusíku. Oxidy dusíku vznikají elektrickými výboji v ovzduší a nitrifikačními bakteriemi, rostliny poté zabudovávají dusičnany do svých buněk jako organický dusík. Rozkladem rostlinných těl se organický dusík formou amoniaku dostává opět do půdy a vody. Činností denitrifikačních bakterií se dusík dostává zpět do vzduchu a tím se koloběh uzavírá (Forejt, 2008).
Člověk svojí činností výrazně zvyšuje obsah dusičnanů v půdě. Dnes je nesrovnatelně vyšší, než býval dříve. Příčinami jsou především zvýšené osídlení krajiny a chemizace zemědělství. Častým používáním vysokých dávek dusíkatých hnojiv se dusičnany dostávají nejen do půdy ale i do povrchových a podzemních vod, následně pak i do pitné vody. Negativně přispívá i růst sídlištních celků. Je tedy prakticky nemožné se dusičnanům vyhnout. Na druhou stranu konzumace dusičnanů v malém množství není pro člověka zdravotně nebezpečná. O jejich vyloučení z moči se z velké části starají naše ledviny, i když u starších lidí je tato funkce o něco menší (Forejt, 2008).
Kontaminace potravin z půdy, formou zemědělských hnojiv se týká hlavně zeleniny. Dle platné legislativy jsou stanoveny limity pro listovou zeleninu dle ročního období a stupně zpracování: např. špenát 2000–3000 mg NO3-/kg. Norma pro pitnou vodu stanovuje nejvyšší mezní hodnotu dusičnanů 50 mg/L NO3- s tím, že tuto normu musí splňovat jak voda balená tak pitná z kohoutku. Pro balenou kojeneckou pitnou vodu je stanovená norma 5x nižší. Nejvyšší množství dusičnanů můžeme očekávat např. ve špenátu, hlávkovém salátu, natích, kedlubně, zelí, či ředkvi (Forejt, 2008, p. 335). Tabulka 20 obsahuje přehled dusičnanů v zelenině.
Tab. 20 Přehled obsahu dusičnanů v zelenině
|
Obsah dusičnanů |
Obsah na kg čerstvé zeleniny |
Běžná zelenina |
|
Velmi vysoký |
2500 mg |
Červená řepa a džus z červené řepy, celer, hlávkový salát, rukola, špenát |
|
Vysoký |
1000-2500 mg |
Čínské zelí, celer, fenykl, pórek, petržel, kedlubna, |
|
Střední |
500-1000 mg |
Zelí, kopr, tuřín, mrkvový džus |
|
Nízký |
200-500 mg |
Brokolice, mrkev, květák, okurka, dýně, |
|
Velmi nízký |
<200 mg |
Chřest, artyčoky, fazolové lusky, fazole, hrách, paprika, rajčata, meloun, batáty, brambory, česnek, cibule, lilek, houby |
Převzato z http://www.ausport.gov.au/__data/assets/pdf_file/0009/466029/Beetroot_juice_Nitrate_11-_website_fact_sheet.pdf
Dle Danihelkové (2010) zelenina ze zimní a předjarní produkce vykazuje vyšší obsahy dusičnanů než z letní sklizně a množství dusičnanů v zelenině nelze ovlivnit ani tepelnou úpravou ani mražením. Danihelková doporučuje odstranit ty části zeleniny, ve kterých je obsah dusičnanů největší, např. středovou část mrkve nebo řapíky u listové zeleniny. Naopak Mgr. Forejt (2008) popisuje možnost docílit snížení obsahu dusičnanů v zelenině 15–30ti minutovým povařením při 95–100 stupních. Ačkoliv vařením, nebo ořezáním zeleniny můžeme v některých případech dosáhnout snížení obsahu dusičnanů, jako nejlepší metoda udržení bezpečnosti potravy se jeví prevence. Plodiny a výrobky z ekologických farem a především sezónní, nerychlená zelenina obsahují jen přirozené množství dusičnanů. Vyšší příjem dusičnanů je pravděpodobnější u vegetariánů.
Dalším zdrojem dusičnanů jsou aditiva, která se používají při zpracování potravin. Jsou to například dusičnan sodný (NaNO3) a dusičnan draselný (KNO3). Používají se pro prodloužení trvanlivosti, jako ochrana před působením některých bakterií (prevence botulismu) a pro udržení stálé barvy. Přidávána jsou především do mas a masných výrobků, ryb a rybích výrobků, konzerv a tvrdých sýrů. Nejvyšší povolená množství těchto aditivních látek jsou určena vyhláškou č. 4/2008 Sb (emulgátory.cz, 2010).
Intenzita zatížení
K měření efektivity suplementace a jejího účinku na svalovou práci se používají zátěžové testy, nejčastěji bicyklový ergometr. Zkoumaní jedinci jsou po konzumaci doplňku obsahujícího nitrát zatěžováni různými intenzitami. Sleduje se odpověď organismu na zátěž. Jedním ze způsobů určení intenzity zatížení je sledování dynamiky laktátu (Jones, 2005b).
Lactate threshold (LT) neboli laktátový práh. Při aktivitě do úrovně laktátového prahu se neprojeví zvýšení laktátu v krvi oproti jeho míře v klidu. Tato intenzita pohybu se může individuálně lišit v rozsahu mezi 50–80% VO2max (Jones, 2005b).
Lactate turnpoint (LTP) neboli bod laktátového obratu. Od tohoto bodu se laktát kumuluje rychleji. Hladina laktátu je přibližně na koncentraci 3-4 mmol/L krve. Intenzita cvičení v oblasti LTP se pohybuje od 70–90% VO2max (Jones, 2005b).
Hladina laktátu je mimo jiné jedním z parametrů určení aerobního a anaerobního prahu, které jsou do určité míry srovnatelné s LT a LTP (Jones, 2005b).
-
Intenzita pod LT se nazývá mírná a je charakterizována pouze mírnou změnou v tvorbě laktátu oproti klidovému stavu (2–2,5 mmol/L). Plicní ventilace stoupá po exponenciální křivce, aby dosáhla rovnovážného stavu po 2–3 minutách u zdravých jedinců. Při této intenzitě, spotřeba kyslíku je přímo úměrná míře obratu ATP v myocytech (kolik ATP se vytvoří, tolik se spotřebuje). Setrvalý stav spotřeby kyslíku má lineární vztah k vnějšímu zatížení a pohybuje se přibližně na hodnotě 10ml O2/min/W. Tato hodnota je jen minimálně ovlivněna věkem a trénovaností a je všeobecně považována za nezměnitelnou dietní nebo farmakologickou intervencí (Bailey et al, 2010b, p. 1394; Jones, 2005b).
-
Konstantní intenzita nad LT ale pod LTP se nazývá střední. Krevní laktát se zvedá nad klidové hodnoty a lehce se snižuje po 10–20 min (většinou do 4 mmol/L). Příjem kyslíku je v průběhu zatížení přibližně konstantní, od začátku cvičení stoupá jenom pozvolna. VO2 se zastavuje výše než by bylo předpokládané množství, lineárně odvozené z hodnoty při mírné intenzitě. Efektivita svalového stahu se postupně snižuje a pomalá komponenta VO2 oddaluje nástup rovnovážného stavu na dobu cca 15 minut od počátku zatížení. Doba zatížení je omezená vyčerpáním svalového glykogenu a termoregulačními změnami. U intenzit nad LT již neplatí hodnota 10 ml na min/W. (Bailey et al, 2010b, p. 1394; Jones, 2005b).
-
Konstantní intenzita nad LTP je označována jako vysoká. Čím větší rychlosti (např. při běhu) je dosaženo nad LTP, tím rychleji stoupá hladina laktátu. Nad touto intenzitou nelze dosáhnout rovnovážného stavu. Od počátku cvičení příjem kyslíku neustále stoupá stejně tak jako laktát. Po dosažení VO2max se rychle zvyšuje hladina laktátu, dokud nedojde k vyčerpání, zpomalení nebo ukončení cvičení. Od překročení LTP dochází ke snižování pH, zvýšenému příjmu O2 a zvýšenému výdeji CO2. Studie zkoumající výsledky zátěžových testů využívají pro svá měření vysokou (kritickou) intenzitu nad tzv. „kritickým výkonem“ (Bailey et al, 2010b, p. 1394; Jones, 2005b).
Kritický výkon je nejvyšší výkon kontinuálně udržitelný, aniž by docházelo ke změnám homeostázy. Kritická intenzita je nejvyšší zátěž pod VO2max, při které je možné dosáhnout dočasného setrvalého stavu příjmu kyslíku. U trénovaných atletů se nachází kolem hodnoty 90–95% VO2max. Tuto intenzitu nelze dlouhodobě udržet. Trénovaný sportovec je schopný udržet intenzitu těsně pod úrovní kritického výkonu pouze po dobu 15–30 minut z důvodu značné spotřeby glykogenu. Intenzitu pohybující se nad tímto prahem budeme nazývat kritická (Bailey et al, 2010b).
Při kritické zátěži nemůže být dosaženo setrvalého stavu příjmu kyslíku, ani krevního laktátu (tvoří se více laktátu, než se spotřebovává) a výkon nad touto hranicí nelze udržet na dobu delší než 10–15 minut (z důvodu vyčerpání). Pomalá komponenta VO2 stoupá k maximálním hodnotám. Dochází k postupnému vyčerpání zásob CrP (kreatinfosfátu), ke klesání pH a zvyšování koncentrace anorganického fosforu (způsobené omezenou tvorbou ATP). Intervence snižující pomalou komponentu VO2 by zvýšily toleranci zátěže takto vysoké intenzity (Jones, 2005b).
Pomalá komponenta VO 2 (neboli pomalá komponenta zotavovacího kyslíku/kyslíkového dluhu) poukazuje na skutečnost, že organismus už nestačí získávat energii oxidativně (Bailey et al, 2010b). Stoupající příjem kyslíku s pokračující zátěží, jak při střední intenzitě (kde se příjem kyslíku nakonec stabilizuje, na hodnotách vyšších než jsou předpokládané hodnoty), tak při vysoké intenzitě (kde spotřeba kyslíku nedosáhne rovnovážného stavu) je znám jako „pomalá komponenta VO2“. Tato veličina poukazuje na kyslíkový dluh, který vzniká při intenzivní fyzické aktivitě. Je to množství kyslíku, které je přijímáno navíc oproti předpokládané hodnotě zjištěné z mírné intensity. Toto množství kyslíku já znázorněno na obrázku 3 (Jones, 2005b).
Obr. 21 Kyslíkový dluh. Šedá barva znázorňuje kyslík přijímaný nad předpokládanou hodnotu.
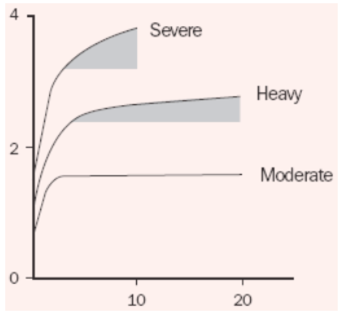
Převzato z http://www.pponline.co.uk/encyc/the-slow-component-of-vo2-understand-it-to-go-faster-39797
Pomalá komponenta VO2 indikuje postupné snižování efektivity využití kyslíku k produkci energie, ačkoliv cvičení probíhá stále stejnou rychlostí. Dokonce, trvá-li výkon dostatečně dlouho, je možné dosáhnout VO2max i když zatížení bylo zahájeno jako sub-maximální. Jakmile je dosaženo VO2max a maximální SF, jediným způsobem jak lze pokračovat v zátěži, je poskytnout dodatečnou (potřebnou) energii anaerobními mechanizmy. Ty mají omezenou kapacitu a výkon tak může být udržen pouze krátkou dobu (Jones, 2005b).
Pomalá komponenta se tedy podílí na vzniku únavy při cvičení. Jak je možné nástup kumulace únavy při cvičení oddálit? Prvním způsobem je důkladné rozcvičení, které připraví organizmus na zátěž. Druhým způsobem je pravidelný vytrvalostní trénink, který ovlivní výši LT a LTP (znázorňuje obrázek č. 4). Jak se ukázalo, třetí možností je využití dietní intervence nitráty (Jones, 2005b).
Obr. 22 Vliv tréninku na spotřebu kyslíku. Na obrázku je vidět rozdíl ve spotřebě kyslíku při běhu stejnou rychlostí před (černé tečky) a po (červené) období tréninku.
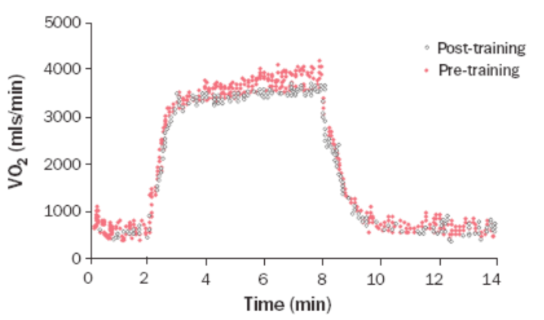
Převzato z http://www.pponline.co.uk/encyc/the-slow-component-of-vo2-understand-it-to-go-faster-39797
Průběh studií
Jako názorný příklad průběhu studie zaměřené na vliv nitrátové suplementace na svalový výkon poslouží práce Baileyho a kol. z roku 2009. Výzkum probíhal formou dvojitě zaslepené studie s kontrolou formou placeba (PL). Osm mužů ve věku 19–38 let pilo 500 ml džusu z červené řepy (ČŘ) obsahující cca 11 mmol nitrátu, nebo 500 ml placeba se zanedbatelným množstvím nitrátu v průběhu 6 po sobě následujících dní a byli vystaveni mírné zátěži na stepperu, z toho poslední 3 dny byla intenzita zátěže kritická. Měřenými parametry byly krevní tlak, zásobení svalů kyslíkem (měřené infračervenou spektroskopií – NIRS) a spotřeba kyslíku. Cílem bylo zjistit jak se tyto parametry při vystavení zátěži mezi PL a ČŘ skupinami.
Dále se využívá stanovení bio-dostupnosti NO v krvi na základě sledování jeho derivátů. Přímé určení množství NO je technicky náročné, a tak se k zjištění koncentrace v krvi používají jeho oxidační produkty nitrit a nitrát. NO3- je relativně inertní, takže biologický efekt je pravděpodobný pouze jeho konverzí na nitrit. Již několikrát bylo prokázáno, že nitrit může být konvertován rychle na NO a je tak považován za nejlepší indikátor bio-dostupnosti NO. Při výzkumu nebyly zjištěny žádné negativní projevy na zdraví u zkoumaných jedinců (Bailey et al, 2009).
Výsledky suplementace nitráty
Konzumace nitrátu z potravinových zdrojů se projevuje vazodilatací, snížením krevního tlaku a snížením spotřeby kyslíku při cvičení. Byla zjištěna zvýšená koncentrace plasmatického NO2-. V souvislosti s touto změnou byl zaznamenán pokles systolického krevního tlaku o cca 8 mmHg (Bailey et al, 2010b, p. 1394). Během další studie stejného autora, v rámci týdenní suplementace nitráty se snížil systolický krevní tlak o 5 mmHg a diastolický o 2 mmHg. Tento efekt je důsledkem zvýšené bio-dostupnosti NO, o které svědčila až dvojnásobná hladina plasmatického nitritu již třetí den. Snížil se příjem kyslíku jak v klidu, tak při mírné, střední i intenzivní zátěži. Hodnoty produkce CO2, minutové ventilace, poměr respirační výměny (využití substrátů se nijak nelišilo), SF ani hladiny laktátu nebyly suplementací nijak ovlivněny ani v klidu ani při zátěži (Bailey et al, 2009, p. 1145).
U mírné zátěže se rozdíl VO2 v klidu a v průběhu zátěže lišil až o 25 % ve prospěch ČŘ skupiny. Měření celkového hemoglobinu ukázalo menší množství oxyhemoglobinu. Při mírné zátěži je v setrvalém stavu příjem kyslíku roven přibližně 10ml O2/min/Wvýkonu při bicyklové ergometrii. Ačkoliv byla tato hodnota považována za neovlivnitelnou věkem, trénovaností i farmakologickou intervencí, ukázalo se, že příjmem dietních, či farmakologických (např. dusičnan sodný) zdrojů nitrátů lze omezit příjem kyslíku z 10,8 ml/min/W na 8,6 ml/min/W. Při velice mírné zátěži o výkonu 20 W k těmto změnám nedochází (Bailey et al, 2009, p 1144).
Porovnáním spotřeby kyslíku u střední intenzity byla zjištěna až o 7 % nižší spotřeba kyslíku u ČŘ skupiny než u skupiny s placebem (Bailey et. al, 2009). Pro vysokou intenzitu zátěže se konzumace nitrátů projevila na prodloužení doby výkonu do vyčerpání. Pomocí snížení pomalé komponenty VO2 (až o polovinu) se podařilo oddálit dosažení VO2max a došlo tedy ke zvýšení tolerance této zátěže (až o 25 %). Během 6 minutové zátěže kritické intenzity se příjem kyslíku lišil o 21 % a celkový příjem kyslíku o 14 %, ačkoliv hodnoty VO2 při ukončení zátěže byly téměř shodné s těmi z PL skupiny. Množství oxyhemoglobinu se nijak nelišilo od PL skupiny (Bailey et. al, 2010a).
Jak v případě mírné, tak při kritické zátěži byl zaznamenán pokles v hladině fosfokreatinu (PCr) a zvýšená schopnost jej šetřit při zátěži, zatímco pH zůstalo nedotčeno. Zlepšení pravděpodobně nastalo zmenšením obratu ATP v pracujících myocytech i při větším výdeji energie a ten tak mohl být pokryt především oxidativní fosforylací (Bailey et. al, 2010a, p. 146).
Použití potravinových nitrátů se ukázalo být funkční v podpoře výkonnosti i v hypoxických podmínkách (např. vysokohorský trénink). AIS (2011) zdůrazňuje nutnost dalšího výzkumu pro ujištění o zdravotní nezávadnosti suplementace a o vyvrácení možnosti vedlejších účinků.
Studie prokázaly zlepšení účinnosti svalové práce (snížení potřeby kyslíku při zatížení) po dlouhodobějším (3–25 dní) i jednorázovém podání řepného džusu. Použitím řepného džusu jako doplňku stravy před fyzickou aktivitou, je možné podpořit odolnost organismu vůči zatížení. Ke zvýšení koncentrace nitrátu v krvi po konzumaci doplňku dochází i u jedinců s vyváženým jídelníčkem, přirozeně obsahujícím dusičnany z různých zdrojů. Tyto studie potvrzují větší účinnost nitrátů v doplňcích stravy oproti pozorované psychologické podpoře (AIS, 2011, p. 2).
Výhody využití NO 3 - oproti L-argininu
Ačkoliv použití doplňku stravy s L-argininem prokázalo 7–10% pokles potřeby kyslíku při fyzické aktivitě střední intenzity, při použití NO3 - bylo za stejných podmínek dosaženo působivějšího, až 19% snížení potřeby kyslíku. Stejně tak použitím L-argininu lze snížit množství krevního laktátu, zvýšit V02max u zdravých jedinců a podpořit toleranci kritické zátěže (až o 20 %), ale použitím nitrátu za stejných podmínek lze dosáhnout až 25% zlepšení tolerance této zátěže. NOS enzymy katalyzující konverzi L-argininu spotřebovávají nutně kyslík, kdežto konverze nitrát-nitrit-oxid dusnatý tento limitující faktor nemá a může tedy probíhat i v hypoxických podmínkách. Použití nitrátu oproti L-argininu se tak pro podporu tolerance zátěže jeví jako vhodnější (Bailey et al, 2010b, p. 1399).
Zajímavostí je, že ve studiích, které neprokázaly uvedené účinky nitrátů nebo l-argininu, se intervence nijak neprojevila na ukazatelích NO syntézy. Nebylo zaznamenáno snížení tlaku krve, ani větší množství nitrátů v moči. Je pravděpodobné, že rozdíly v účincích mohou být dány režimem suplementace. Po jedné větší dávce nitrátu/l-argininu se koncentrace nitritu v krevní plazmě změní znatelněji, než při pravidelných menších dávkách v průběhu dne. Při dlouhotrvající, 3–14ti denní suplementaci L-arg došlo k navýšení produkce jeho přirozeného rozpadového metabolitu (asymetrický dimethylarginin), který může působit inhibičně na všechny formy NOS. Na rozdílných výsledcích se může podílet i různé načasování cvičební jednotky ve vztahu ke konzumaci doplňku. Zvláště při pravidelném dlouhodobém dávkování je nepravděpodobné, že by byla přijata dostatečně velká dávka účinné látky (v tomto případě L-arg), která by dostatečně ovlivnila bio-dostupnost NO, snížila krevní tlak a pozitivně ovlivnila fyziologické odpovědi organismu na cvičení. Jako optimálnější volba se tedy jeví jednorázová dávka s větším obsahem účinných látek 1–2 hodiny před cvičením, oproti pravidelnému příjmu nitrátů nebo L-argininu v podobně několika menších dávek v průběhu dne (Bailey et al, 2010b, p. 1400).
Mechanismus účinku NO na svalovou práci
Zvýšená tvorba NO způsobuje větší prokrvení, lepší přístup kyslíku k tkáním a umožňuje v úvodu cvičení vysoké intenzity přijímat rychleji větší množství kyslíku. Oproti nižší intenzitě je tedy v první fázi cvičení znát větší VO2. Manipulace s tvorbou NO omezuje růst pomalé komponenty VO 2. S tím se pojí menší míra svalové únavy (např. důsledkem pomalejší kumulace laktátu) a změna zapojení motorických jednotek. Čím větší počet motorických jednotek se zapojí, tím menší měrou dochází k jejich únavě (Bailey et al, 2010b). Zlepšením dynamiky VO2 snížením pomalé komponenty je předpokládáno ušetření anaerobních rezerv a omezení tvorby metabolitů související s procesem vzniku únavy (Bailey et al, 2010b, p. 1400).
Mechanismus ovlivnění tolerance zátěže se zdá být jasný. S jednou výjimkou. Jak je možné, že NO derivované z nitritu ovlivňuje příjem kyslíku při zátěži? Redukce NO2- je usnadněna hypoxií. Více NO se tvoří právě v oblastech svalů, ke kterým se dostává méně kyslíku, nebo ho více využívají. Tento mechanismus pomáhá vyrovnat potřebu krve v dané oblasti a zajistit rovnoměrnější rozdělení kyslíku ve svalech. Lepší prokrvení je prospěšné pro funkci svalu, ale nevysvětluje snížený příjem 02 a jeho sníženou spotřebu ve svalech. (Bailey et al, 2010b)
Na základě snížení spotřeby kyslíku při cvičení střední intenzity, pomocí suplementace nitráty autoři studie (Bailey et al, 2010b, p. 1400) usoudili, že zvýšená tvorba NO touto dietní intervencí vyvolává zdokonalení efektivity svalové práce, pravděpodobně snížením potřeby O2 na produkci ATP (efektivnější svalová práce), nebo snížením potřeby O2 na resyntézu ATP (podpořená míra mitochondriální fosforylace ADP na VO2) nebo oběma mechanismy.
Ze značně sníženého celkového obratu ATP u těchto měření vyplývá nižší cena produkce síly na jednotku ATP. Jinými slovy zdá se, že suplementace nitráty umožňuje působit stejnou silou, se sníženými nároky na kyslík a energii (Bailey et al, 2010a).
Přesný mechanismus účinku je stále nejasný, ale aby mohlo dojít ke snížení potřeby kyslíku, NO by musel v těle splňovat tyto funkce:
-
Zpomalit resyntézu ATP v mitochondriích – Buď omezením „prokluzování“ na mitochondriálních protonových pumpách, nebo rolí nitiritu jako alternativního akceptoru elektronu.
-
Snížit potřebu ATP na produkci síly
-
Zbrzdit tvorbu ATP v mitochondriích.
Zdá se, že snížená potřeba kyslíku se projevuje pouze v průběhu kontrakcí kosterního svalstva, jinak by byla výrazně změněna hodnota VO2 v klidu. Změny mitochondriální aktivity probíhají pravděpodobně pouze v kosterním svalstvu a jsou výsledkem zlepšení efektivity svalového stahu, ne zdokonalením respiračních procesů (Bailey et al, 2010a).
Využití suplementace při zdravotním oslabení
Znalosti o účincích nitrátu by bylo možné využít pro zdravotní účely. K oslabené funkci endotelu dochází stárnutím a rozvojem různých patologií. Tím je omezena schopnost tvorby NO, což by mohlo vysvětlovat sníženou zátěžovou výkonnost v těchto populacích. L-arg a NO3- pomáhají prodloužit vzdálenost, jakou dokáží v kuse ujít pacienti s periferní arteriální chorobou (většinou ischemická onemocnění dolních končetin, která postihují kolem 20 % populace starší 60 let) a podporují zátěžovou toleranci u pacientů s chronickým srdečním selháváním (Bailey et al, 2010b, p. 1400).
V populacích zasažených kardiovaskulárními, respiračními nebo metabolickými poruchami se v každodenním životě objevují fyzicky náročné situace se značnými požadavky na energii. Tyto požadavky tvoří velkou část jejich VO2max a jsou tedy značnou zátěží. Snížení spotřeby kyslíku v těchto situacích má potenciál podpořit schopnost tolerance takové zátěže a tím pozitivně ovlivnit kvalitu života v omezených skupinách (Bailey et al, 2009, p. 1153).
Další funkce oxidu dusnatého
Oxid dusnatý stimuluje vazodilataci. V kardiovaskulárním systému se oxid dusnatý podílí na udržování tonu cév a krevního tlaku, inhibuje adhesi (přilnavost) a i agregaci (shlukování) trombocytů, tlumí aktivaci leukocytů, má antiproliferační (působí proti bujení) účinek a inhibuje apoptózu. Relaxuje střevní hladkou svalovinu, včetně svěračů a prostřednictvím vazodilatace způsobuje například i erekci. NO je důležitý pro správnou funkci ledvin a má klíčový význam pro obranné schopnosti mukózní vrstvy gastrointestinálního traktu (ta chrání střevní stěnu před poškozením např. trávicími šťávami). NO má v krvi především ochrannou úlohu. Zodpovídá za neustálé udržování základní dilatace cév v arteriálním řečišti. V imunitním systému se účastní nespecifické obrany (hlavně proti prvokům, některým bakteriím, virům a nádorům), zasahuje do procesu fagocytózy a zánětu, podílí se na ochraně funkční kapacity endotelu, prevenci aterosklerózy, cévních poškození a hypertenze (Asano, 2012, p. 76; Kupková & Beneš, 2004, p. 117).
NO je mediátorem v CNS a je považován za jeden z mediátorů bolesti. Podporuje vaskulární relaxaci, snižuje srdeční předpětí i dotížení, hypertrofii myokardu a dysfunkci levé srdeční komory (Nicox Company, 2012).
Pro udržení fyziologického krevního tlaku je nutná správná funkce ledvin. NO se podílí na regulaci průtoku krve ledvinami působením přímo v nefronech, kde ovlivňuje reabsorpci sodíku a bikarbonátu a zároveň blokuje produkci reninu, který prostřednictvím renin-angiotensin systému zajišťuje vazokonstrikci (Nicox Company, 2012).
Regulace funkce GI traktu
V gastrointestinálním traktu se podílí na udržování střevní motility. Kontrakce probíhající ve střevech jsou řízeny inhibičními a excitačními motorickými neurony, které zajišťují inervaci hladkého svalstva. NO produkované nNOS v těchto neuronech zajišťuje relaxaci buněk hladké svaloviny tak, aby následovala po kontrakci, což umožňuje normální peristaltiku. Deficit v tvorbě NO je jedním z průvodních, pozorovatelných projevů poruch GI motility jako například u hypertrofické stenózy pyloru, diabetické enteropatie, nebo tzv. „slow transit“ zácpě. Vnitřní povrch trávicího ústrojí je neustále napadán dráždivými látkami z potravy, alkoholu, léků a endogenní sekrecí žaludeční kyseliny, trávicích šťáv a žluči. Ochranou vůči těmto vlivům je hlen (produkovaný buňkami trávicího traktu), který tvoří bariéru mezi lumenem střeva a jeho sliznicí. NO podporuje sekreci mucinu, tvořícího hlen a obnovu této vrstvy po poškození (Nicox Company, 2012).
Relaxace cév
Vyprodukovaný NO rozšiřuje všechny typy cév tak, že projde jednoduchou difúzí z endotelových buněk do buněk hladké svaloviny. Tam se váže na železo hemu v cytosolové guanilátcykláze (GC) a výsledkem je zvýšení koncentrace guanizinmonofosfátu (cGMP), která vede ke snížení vnitrobuněčné koncentrace Ca 2+ a k defosforylaci lehkých řetězců myozinu a tím k uvolnění buněk hladkého svalstva cév (Púzserová, 2008, p. 56).
Basální sekrece NO funguje jako antagonista působení sympatiku. Je hlavním dilatačním mechanismem, který dlouhodobě udržuje propustnost cév. (Kuneš et al, 2004) Čím větší je průměr cévy, tím větší je množství NO vyloučeného pro její relaxaci (Púzserová, 2008, p. 56).
Arteriální a venózní systém se od sebe liší strukturou i funkcí. Žíly nejsou neustále dilatované účinkem NO, ale v případě potřeby reagují na menší množství. Proto se nitro-preparáty, z kterých se uvolňuje NO, dosáhne venodilatace, tj. poklesu žilního tlaku krve, a tím optimalizace průtoku krve (Štvrtinová, et al, 1998, p. 8).
Pro léčbu akutních i subakutních plicních hypertenzních stavů je úspěšně používána inhalace NO (Kupková & Beneš, 2004, p. 117).
Antiagregační mechanismus
NO po svojí syntéze difunduje do hladké svaloviny, kde vyvolává relaxaci a omezení dělení buněk hladké svaloviny, ale současně i na povrch endotelu, kde tlumí přilnavost a shlukování krevních destiček i některých bílých krvinek (neutrofilů). Tento mechanismus obecně zabraňuje srážení krve v cévách. Trombocyty mají vlastní způsoby produkce NO, kterými regulují svou přilnavost (Štvrtinová, et al, 1998, p. 8).
Vliv NO na regeneraci
Produkce NO má vliv na mobilizaci tzv. CPC buněk (circulating progenitor cells neboli myosatelitní buňky, ze kterých dále vznikají buňky kosterního svalstva), které působí jako potenciální mediátory svalové regenerace. Sekrece CPC je přímo závislá na dostatku NO. Neurální NOS zvyšuje svou aktivitu během svalových kontrakcí. Takto tvořený NO podporuje proliferaci CPC a buněk kosterní svaloviny. Nedostatek NO může přispívat k neadekvátní rovnováze mezi cévním poškozením a mechanismy svalové regenerace a má tedy vliv i na tvorbu svalové tkáně, případně na vznik svalové atrofie (Asano, 2012, p. 80).
Patologické funkce NO
V těle se oxid dusnatý objevuje i při nežádoucích reakcích s poškozujícím účinkem. Ve většině případů se patologie týká jeho nadbytku nebo nedostatku. Protože NO se vyskytuje jako radikál, za přístupu vzduchu rychle reaguje s kyslíkem a dává tak vzniknout některým nebezpečným látkám. Například oxid dusičitý (NO2, vzniká ve spalovacích motorech a je součástí kyselých dešťů) může reakcí s mastnými kyselinami tvořit karcinogenní látky a reakcí s tyrosinem vést k destrukci tkání. Reakcí NO se superoxidem (O2-) vzniká toxický peroxodusitan (OONO-) jehož toxicita pramení z oxidace atomů železa a síry v bílkovinách. Peroxidace lipidů může vést až k poškození DNA a apoptóze (programovaná smrt buňky). (Kupková & Beneš, 2004, p. 117).
Přemíra NO je typickým průvodním znakem septického šoku a pravděpodobně bude klíčovou molekulou vaskulárně podmíněných bolestí hlavy. Dále je spojována s rozvojem Alzheimerovy choroby, epilepsie, a se zánětlivým onemocněním střev (Kupková & Beneš, 2004, p. 117). Nadměrná aktivita iNOS je typická u artritid a při bronchiálním astmatu, kde se hladina vydechovaného NO využívá jako jeden z ukazatelů zánětu dýchacích cest. Patologicky snížená i zvýšená produkce NO se uplatňuje u očních chorob. Snížená koncentrace NO je jedním z faktorů hypertenze a erektilní dysfunkce (Kupková & Beneš, 2004, p. 118). Dle Sedláčka (1999) se NO projevuje i v glutamátové neurotoxicitě.
Methemoglobinémie
Reakcí NO se železem v erytrocytech vzniká methemoglobin (Kupková & Beneš, 2004, p. 117). Methemoglobin je forma hemoglobinu, která není schopná vázat kyslík. Při zvýšené koncentraci v krvi způsobuje funkční anémii a tím hypoxii tkání (Ash-Bernal, et al, 2004, p. 4). Methemoglobinémie se často objevuje u malých dětí, kojenců, zvláště do tří měsíců v oblastech s vyšším obsahem dusičnanů v pitné vodě. Dětský organismus není schopen dlouhodobě redukovat množství methemoglobinu, objevuje se cyanóza (modravé zbarvení sliznic a pokožky okrajových částí těla) a u kojenců může dojít až k udušení (Rodová, 2011, p. 23). Dále se projevuje zvýšením tepové frekvence, rychlosti dýchání a snížením krevního tlaku (Forejt, 2008, p. 335).
Molekula oxidu dusnatého zajišťuje organismu regulaci důležitých funkcí od trávení a imunitních reakcí až po udržování krevního zásobení a regenerace svalových buněk. Je-li NO v nadbytku, reaguje ve zvýšené míře s kyslíkovými radikály a produkty této reakce mají poškozující účinky na tkáně. Nedostatečné množství NO se projevuje poruchami prokrvení, zvýšenou krevní srážlivostí a vyšším krevním tlakem. Rovnováha v tvorbě a využití NO je nutná pro správné fungování všech orgánových systémů.